Korozja to wszechobecne zjawisko, które stopniowo niszczy materiały wokół nas. Ten artykuł wyjaśni, czym jest korozja, jakie są jej mechanizmy i czynniki przyspieszające, a także przedstawi skuteczne metody ochrony, pomagając zrozumieć, jak chronić nasze otoczenie przed jej niszczycielskim wpływem.
Korozja to naturalne niszczenie materiałów poznaj jej mechanizmy i wpływ na otoczenie.
- Korozja to proces stopniowego niszczenia materiałów, głównie metali, w wyniku reakcji chemicznych lub elektrochemicznych ze środowiskiem.
- Wyróżnia się dwa główne typy: korozję chemiczną (w środowisku suchym, wysokich temperaturach) i elektrochemiczną (najczęściej spotykaną, z udziałem elektrolitu, np. wody).
- Główne czynniki przyspieszające to wilgotność, tlen, zanieczyszczenia atmosferyczne (kwaśne deszcze), sole (drogowe), wysoka temperatura oraz kontakt różnych metali.
- Skutki korozji są znaczące: obejmują straty ekonomiczne (nawet 4-5% PKB w Polsce), zagrożenia bezpieczeństwa konstrukcji oraz utratę wartości estetycznej.
- Najskuteczniejsze metody ochrony to powłoki ochronne (farby, cynkowanie), ochrona katodowa, stosowanie stali nierdzewnych oraz inhibitory korozji.
Rdza, nalot, patyna jak rozpoznać proces niszczenia materiałów?
Korozja to nic innego jak proces stopniowego niszczenia materiałów. Choć najczęściej kojarzymy ją z metalami i ich stopami, takimi jak żelazo czy miedź, to zjawisko to dotyka również betonu, a nawet skał. W swojej istocie korozja jest naturalnym dążeniem materiału do powrotu do jego pierwotnej, bardziej stabilnej termodynamicznie formy, w jakiej występował w rudach. Kiedy wydobywamy metal z ziemi i przetworzymy go na użyteczny przedmiot, w pewnym sensie "zmuszamy" go do przyjęcia stanu o wyższej energii. Korozja to po prostu jego "chęć" powrotu do naturalnej równowagi.
Na co dzień widzimy różne manifestacje tego procesu. Najbardziej oczywistym przykładem jest rdza, czyli czerwono-brązowy nalot na żelazie i stali. Ale korozja to także zielonkawa patyna na miedzianych dachach czy pomnikach, czy też ciemny nalot na srebrze. Wszystkie te zjawiska to widoczne efekty reakcji chemicznych lub elektrochemicznych metalu z otaczającym go środowiskiem.
Korozja jako naturalny proces: dlaczego metale chcą "wrócić do korzeni"?
Z punktu widzenia termodynamiki, metale w stanie czystym lub jako stopy, które zostały poddane obróbce i formowaniu, są w stanie energetycznie mniej stabilnym niż ich związki, z których pierwotnie zostały wydobyte. Wyobraźmy sobie rudę żelaza to stabilny tlenek. Aby uzyskać z niej czyste żelazo, musimy dostarczyć dużo energii. To jak "wypchnięcie" metalu na wyższy poziom energetyczny. Korozja jest więc naturalnym procesem, w którym metal dąży do obniżenia swojej energii, powracając do bardziej stabilnych form, takich jak tlenki czy siarczki, które są jego "korzeniami" w naturze. To nie jest "złośliwość" materiału, a po prostu nieuchronne prawo natury.
Skala problemu w Polsce: jak wilgotny klimat i smog wpływają na tempo niszczenia?
W Polsce problem korozji jest szczególnie dotkliwy, a my, jako społeczeństwo, ponosimy z tego tytułu ogromne koszty. Nasz klimat, charakteryzujący się wysoką wilgotnością powietrza i zmiennymi temperaturami, tworzy idealne warunki do rozwoju procesów korozyjnych. Dodatkowo, w rejonach przemysłowych i dużych miastach, zanieczyszczenia atmosferyczne, takie jak tlenki siarki i azotu (składniki smogu), drastycznie przyspieszają niszczenie materiałów. To właśnie te czynniki sprawiają, że korozja jest u nas zjawiskiem niezwykle powszechnym i intensywnym.
Szacuje się, że straty ekonomiczne spowodowane korozją w Polsce mogą sięgać nawet 4-5% Produktu Krajowego Brutto. Co się na to składa? To gigantyczne koszty związane z koniecznością regularnej wymiany skorodowanych elementów infrastruktury (mostów, rurociągów, słupów energetycznych), napraw pojazdów i maszyn, a także ciągłego stosowania różnego rodzaju zabezpieczeń. To ogromne obciążenie dla gospodarki, które często pozostaje niewidoczne dla przeciętnego obywatela, dopóki nie zobaczy zardzewiałej barierki czy zniszczonego samochodu.
Dwa główne typy korozji jak materiały ulegają zniszczeniu?
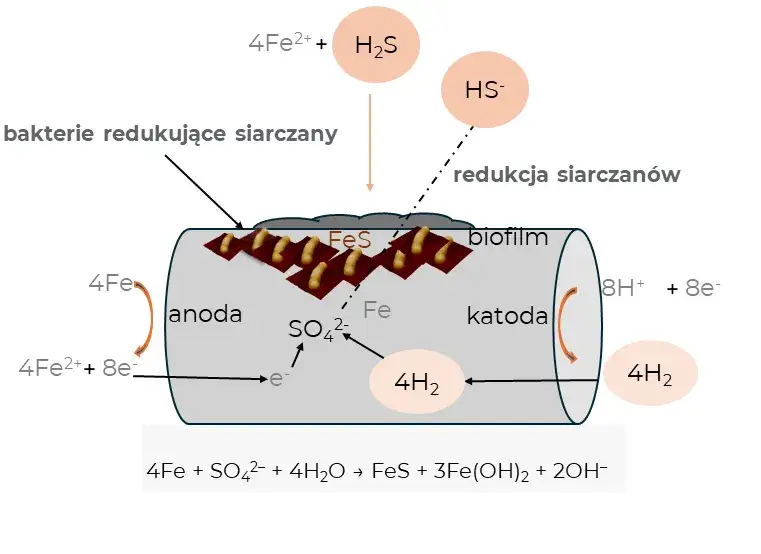
Chociaż korozja jest jednym zjawiskiem, możemy wyróżnić dwa główne mechanizmy, które prowadzą do niszczenia materiałów: korozję chemiczną i korozję elektrochemiczną. Zrozumienie różnic między nimi jest kluczowe, aby skutecznie z nimi walczyć.
Korozja chemiczna: gdy wysoka temperatura i gazy stają się wrogiem
Korozja chemiczna to typ korozji, który zachodzi bez udziału ciekłego elektrolitu. Dzieje się tak zazwyczaj w środowisku suchym, ale za to w wysokich temperaturach i w obecności agresywnych gazów, takich jak tlen, siarka czy chlor. W tych warunkach metal bezpośrednio reaguje z gazami, tworząc na swojej powierzchni związki, które często są kruche i nie zapewniają ochrony. Klasycznym przykładem jest utlenianie stali w piecach hutniczych, gdzie wysokie temperatury i obecność tlenu prowadzą do tworzenia się grubej warstwy tlenków, czyli tzw. zgorzeliny. Ten rodzaj korozji jest mniej powszechny w codziennym życiu, ale ma ogromne znaczenie w przemyśle, zwłaszcza w procesach wysokotemperaturowych.
Korozja elektrochemiczna: jak niewidoczne ogniwa elektryczne zjadają metal?
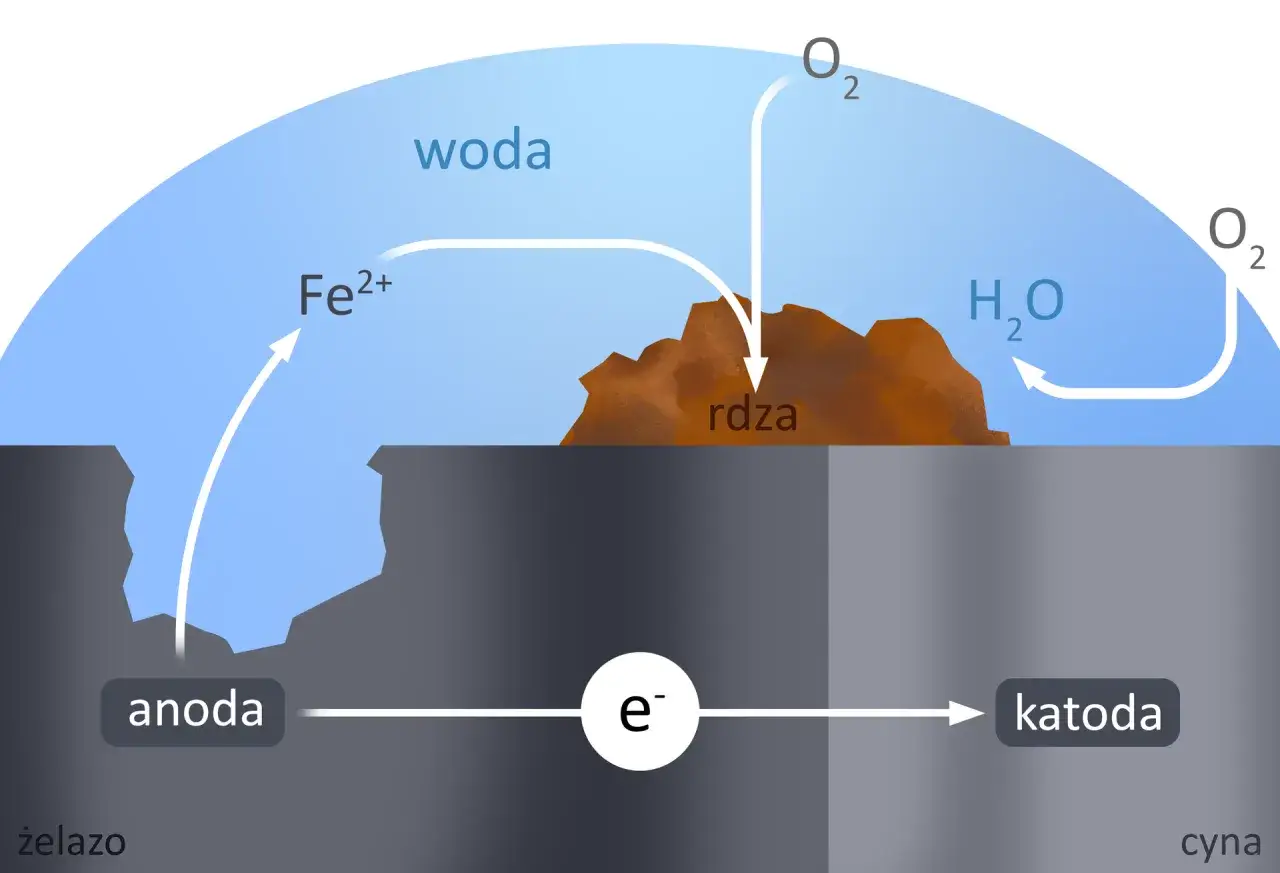
To właśnie korozja elektrochemiczna jest tym typem, z którym spotykamy się najczęściej to ona odpowiada za rdzewienie żelaza czy niszczenie karoserii samochodów. Jej kluczową cechą jest obecność elektrolitu, czyli cieczy przewodzącej prąd, najczęściej wody z rozpuszczonymi w niej solami. Na powierzchni metalu, w kontakcie z elektrolitem, tworzą się maleńkie, niewidoczne gołym okiem mikroogniwa galwaniczne. Działają one jak miniaturowe baterie, w których zachodzą reakcje chemiczne prowadzące do niszczenia metalu.
W tych mikroogniwach wyróżniamy dwa obszary:
- Anoda: To miejsce, gdzie metal ulega utlenianiu, czyli rozpuszczaniu. Jest to obszar, który jest "zjadany" przez korozję.
- Katoda: Tutaj zachodzą reakcje redukcji, najczęściej tlenu (w środowisku obojętnym lub zasadowym) lub wodoru (w środowisku kwaśnym). Metal w tym miejscu nie ulega niszczeniu, a wręcz jest chroniony.
Przepływ elektronów między anodą a katodą, możliwy dzięki przewodnikowi (samemu metalowi) i elektrolitowi, jest istotą procesu korozji elektrochemicznej. To dlatego wilgotne środowisko jest tak niebezpieczne dla metali.
Anoda i katoda na jednej powierzchni co to jest mikroogniwo korozyjne?
Zjawisko mikroogniwa korozyjnego jest fascynujące, a jednocześnie niezwykle destrukcyjne. Nie potrzebujemy dwóch różnych metali, aby powstało ogniwo galwaniczne. Wystarczy, że na powierzchni jednego metalu pojawią się różnice w składzie, strukturze, naprężeniach, a nawet w dostępie do tlenu. Te różnice sprawiają, że różne obszary tej samej powierzchni zaczynają pełnić funkcje anody i katody. Na przykład, w miejscu, gdzie jest mniej tlenu (szczelina, pod kroplą wody), metal może stać się anodą i ulegać rozpuszczaniu, podczas gdy obszary z lepszym dostępem do tlenu stają się katodami. To prowadzi do lokalnego, często bardzo intensywnego niszczenia materiału, co jest szczególnie niebezpieczne, bo może prowadzić do powstawania wżerów i perforacji.
Rola wody i elektrolitów: dlaczego wilgoć jest największym sprzymierzeńcem rdzy?
Woda jest absolutnie kluczowa dla korozji elektrochemicznej. Działa ona jako elektrolit, umożliwiając przepływ jonów i zamykając obwód elektryczny mikroogniwa. Sama czysta woda nie jest idealnym przewodnikiem, ale w naturze rzadko mamy do czynienia z idealnie czystą wodą. Rozpuszczone w niej sole, takie jak chlorki (np. z soli drogowej, zanieczyszczeń morskich), drastycznie zwiększają jej przewodnictwo. Im wyższe przewodnictwo elektrolitu, tym łatwiejszy przepływ prądu w mikroogniwach, a co za tym idzie szybciej postępuje proces niszczenia.
Dlatego właśnie wilgoć jest największym sprzymierzeńcem rdzy. Warto wiedzieć, że proces korozji elektrochemicznej na żelazie znacznie przyspiesza, gdy wilgotność względna powietrza przekracza około 60%. Poniżej tego progu, choć korozja może zachodzić, to jest ona znacznie wolniejsza. To dlatego w suchych warunkach metale rdzewieją znacznie wolniej niż w wilgotnych.
Czynniki przyspieszające korozję co sprzyja niszczeniu?
Zjawisko korozji to złożony proces, na który wpływa wiele czynników. Niektóre z nich są niezbędne do jego zajścia, inne zaś drastycznie przyspieszają jego tempo. Jako ekspert w tej dziedzinie, mogę z całą pewnością stwierdzić, że zrozumienie tych czynników jest pierwszym krokiem do skutecznej ochrony.
Wilgoć i tlen: duet niezbędny do powstania rdzy
Jak już wspomniałem, woda i tlen to absolutne minimum, aby żelazo zaczęło rdzewieć. Woda pełni rolę elektrolitu, czyli środowiska, w którym jony mogą swobodnie się przemieszczać. Tlen natomiast działa jako depolaryzator katodowy jest on redukowany na katodzie, co umożliwia dalsze utlenianie żelaza na anodzie. Bez tlenu reakcje katodowe są znacznie spowolnione, a co za tym idzie, proces rdzewienia jest zahamowany. Dlatego też, jeśli chcemy chronić żelazo przed korozją, musimy odciąć mu dostęp do jednego z tych dwóch czynników, a najlepiej do obu.
Kwaśne deszcze i zanieczyszczenia przemysłowe: cichy zabójca metali w miastach
Zanieczyszczenia atmosferyczne to prawdziwa plaga naszych czasów, a ich wpływ na korozję jest niedoceniany. Tlenki siarki (SO₂) i azotu (NOx), emitowane przez przemysł i transport, reagują z wodą w atmosferze, tworząc kwasy głównie siarkowy i azotowy. Te kwasy spadają na ziemię w postaci tzw. kwaśnych deszczy. Kiedy taka kwaśna woda osiada na powierzchni metalu, staje się ona niezwykle agresywnym elektrolitem. Kwaśne środowisko drastycznie przyspiesza procesy korozyjne, ponieważ sprzyja reakcjom redukcji wodoru na katodzie, co z kolei napędza utlenianie metalu. To cichy zabójca, który niezauważalnie, ale skutecznie niszczy naszą infrastrukturę w miastach i rejonach przemysłowych.
Sól drogowa zimą: dlaczego samochody rdzewieją w ekspresowym tempie?
Każdy właściciel samochodu wie, jak destrukcyjny wpływ ma zima na karoserię. Winowajcą jest sól drogowa, a dokładniej chlorki, które są jej głównym składnikiem. Chlorki mają podwójnie negatywny wpływ na metale. Po pierwsze, znacząco zwiększają przewodnictwo wody, tworząc bardzo efektywny elektrolit. Po drugie, i to jest szczególnie niebezpieczne, jony chlorkowe mogą niszczyć naturalne warstwy pasywne, które chronią niektóre metale (np. stal nierdzewną czy aluminium). Kiedy taka warstwa zostanie naruszona, korozja może postępować w ekspresowym tempie, prowadząc do powstawania głębokich wżerów i perforacji. Dlatego tak ważne jest regularne mycie samochodu zimą, aby usunąć szkodliwe osady soli.
Niebezpieczne sąsiedztwo: jak kontakt różnych metali przyspiesza ich degradację
Zjawisko korozji galwanicznej to coś, co powinien znać każdy projektant i wykonawca. Kiedy dwa różne metale o odmiennych potencjałach elektrochemicznych (czyli o różnej "szlachetności") zostaną ze sobą połączone i znajdą się w obecności elektrolitu, powstaje ogniwo galwaniczne. Metal mniej szlachetny (czyli ten o niższym potencjale, np. żelazo w kontakcie z miedzią) staje się anodą i ulega przyspieszonej korozji, podczas gdy metal szlachetniejszy (katoda) jest chroniony. To dlatego nie powinno się łączyć miedzianych rur ze stalowymi bez odpowiedniej izolacji. Niewłaściwe zestawienie metali to prosta droga do szybkiej degradacji jednego z nich.
Konsekwencje korozji wpływ na bezpieczeństwo i finanse.
Korozja to nie tylko problem estetyczny czy ekonomiczny. Jej skutki mogą być znacznie poważniejsze, wpływając bezpośrednio na bezpieczeństwo ludzi i środowiska. Jako inżynier, widziałem wiele przypadków, gdzie zlekceważenie korozji prowadziło do tragicznych konsekwencji.
Od dziury w płocie do katastrofy budowlanej: jak korozja wpływa na bezpieczeństwo?
- Osłabienie wytrzymałości konstrukcji nośnych, takich jak mosty, wiadukty czy elementy budynków, prowadzi do ryzyka nagłych awarii i katastrof budowlanych. Zardzewiałe zbrojenie w betonie traci swoją nośność, a skorodowane elementy stalowe mogą po prostu pęknąć pod obciążeniem.
- Awarie instalacji, w tym rurociągów transportujących wodę, gaz, ropę czy chemikalia, oraz zbiorników magazynujących te substancje. Mogą one skutkować wyciekami, które z kolei prowadzą do zanieczyszczenia środowiska, pożarów, a nawet eksplozji.
- Zagrożenie dla bezpieczeństwa pojazdów i maszyn, wynikające z osłabienia kluczowych elementów, takich jak układy hamulcowe, zawieszenie czy elementy konstrukcyjne. Korozja może sprawić, że pozornie sprawny pojazd stanie się śmiertelnym zagrożeniem na drodze.
Ukryte koszty rdzy: dlaczego straty gospodarcze liczone są w miliardach?
Ekonomiczne skutki korozji są naprawdę porażające i często niedoceniane. Jak już wspomniałem, w Polsce straty te szacuje się na 4-5% PKB, co przekłada się na miliardy złotych rocznie. Te koszty nie wynikają jedynie z konieczności wymiany skorodowanych elementów. Składają się na nie również:
- Koszty napraw i konserwacji: Regularne malowanie, czyszczenie, wymiana drobnych elementów.
- Koszty zabezpieczeń: Inwestycje w powłoki ochronne, inhibitory, systemy ochrony katodowej.
- Straty wynikające z przestojów: Awarie spowodowane korozją często wymagają wyłączenia z użytku całych linii produkcyjnych, mostów czy rurociągów, co generuje ogromne straty dla przedsiębiorstw i gospodarki.
- Koszty utylizacji: Zniszczone przez korozję elementy muszą zostać zutylizowane, co również generuje koszty.
To pokazuje, że walka z korozją to nie tylko kwestia techniczna, ale również strategiczna dla rozwoju gospodarczego i bezpieczeństwa.
Estetyka ma znaczenie: jak procesy korozyjne wpływają na wygląd naszego otoczenia?
Choć może się to wydawać mniej istotne niż bezpieczeństwo czy finanse, estetyka otoczenia również ma znaczenie. Rdzewiejące elementy psują wygląd budynków, pojazdów, infrastruktury miejskiej, a także przedmiotów codziennego użytku. Zardzewiała barierka, skorodowana elewacja czy samochód z widocznymi ogniskami rdzy obniżają wartość wizualną i funkcjonalną. W przestrzeni publicznej wpływa to na ogólne wrażenie zaniedbania i może obniżać jakość życia mieszkańców. W przypadku produktów konsumenckich, korozja szybko obniża ich wartość rynkową i zaufanie do marki. Dbałość o estetykę jest więc również elementem walki z korozją.
Skuteczne metody ochrony przed korozją jak zapobiegać niszczeniu?
Skoro wiemy już, czym jest korozja i jak destrukcyjny ma wpływ, naturalne jest pytanie: jak możemy się przed nią bronić? Na szczęście, inżynieria materiałowa i chemia oferują szereg skutecznych metod ochrony, które pozwalają znacząco wydłużyć żywotność materiałów.
Bariera nie do przejścia: rola powłok ochronnych w walce z korozją
Powłoki ochronne to najpopularniejsza i najbardziej podstawowa metoda walki z korozją. Ich głównym zadaniem jest stworzenie fizycznej bariery, która izoluje metal od agresywnego środowiska zewnętrznego. Dzięki temu czynniki korozyjne, takie jak woda, tlen czy zanieczyszczenia, nie mają bezpośredniego kontaktu z powierzchnią metalu, co skutecznie zapobiega inicjacji i rozwojowi korozji.
Farby, lakiery i emalie najpopularniejsze metody zabezpieczania
Wśród powłok ochronnych wyróżniamy kilka głównych typów:
- Niemetaliczne organiczne: Do tej grupy zaliczamy przede wszystkim farby, lakiery i tworzywa sztuczne. Tworzą one warstwę, która nie tylko izoluje metal, ale często również nadaje mu pożądany wygląd. Są stosunkowo łatwe w aplikacji i stanowią pierwszą linię obrony dla wielu konstrukcji i przedmiotów.
- Niemetaliczne nieorganiczne: Tutaj mamy do czynienia z emaliami, powłokami ceramicznymi czy fosforanowaniem. Charakteryzują się one znacznie wyższą odpornością chemiczną i mechaniczną niż powłoki organiczne, co sprawia, że są idealne do zastosowań w trudniejszych warunkach, np. w wysokich temperaturach czy w środowiskach agresywnych chemicznie.
Cynkowanie i chromowanie: metal w obronie metalu
Inną grupą są metaliczne powłoki ochronne, które polegają na pokrywaniu jednego metalu warstwą innego. Najbardziej znanym przykładem jest cynkowanie. Cynk, będąc metalem mniej szlachetnym niż żelazo, zapewnia tzw. ochronę protektorową (galwaniczną). Oznacza to, że w przypadku uszkodzenia powłoki, to cynk będzie korodował jako pierwszy, "poświęcając się" w obronie chronionego żelaza. To niezwykle skuteczna metoda, szeroko stosowana w budownictwie, motoryzacji czy przy produkcji ogrodzeń.
Inne popularne powłoki metaliczne to chromowanie i niklowanie. Te metody tworzą twarde, odporne na korozję i ścieranie powierzchnie, które dodatkowo są bardzo estetyczne, co jest ważne w przemyśle motoryzacyjnym czy przy produkcji elementów dekoracyjnych.
Ochrona katodowa: zaawansowana technologia dla statków, mostów i rurociągów
Ochrona katodowa to bardziej zaawansowana metoda, stosowana głównie do ochrony dużych i strategicznych konstrukcji, takich jak rurociągi, statki, zbiorniki podziemne czy elementy mostów. Polega ona na uczynieniu chronionej konstrukcji katodą ogniwa galwanicznego. Można to osiągnąć na dwa sposoby:
- Metoda protektorowa: Polega na połączeniu chronionej konstrukcji z zewnętrzną anodą (protektorem) wykonaną z metalu mniej szlachetnego (np. magnezu, cynku). Protektor koroduje zamiast chronionej konstrukcji.
- Metoda z zewnętrznym źródłem prądu: W tym przypadku do chronionej konstrukcji doprowadzany jest prąd z zewnętrznego źródła, co wymusza jej katodowe zachowanie, a anoda jest wykonana z materiału odpornego na korozję (np. grafitu).
To niezwykle skuteczna technologia, która pozwala znacząco wydłużyć żywotność konstrukcji pracujących w agresywnych środowiskach, takich jak woda morska czy gleba.
Stal nierdzewna: czy istnieje materiał całkowicie odporny na korozję?
Stal nierdzewna, czyli stopy żelaza z chromem i często niklem, to przykład materiału o znacznie podwyższonej odporności na korozję. Jej niezwykła właściwość wynika z mechanizmu samoczynnego tworzenia cienkiej, szczelnej i trwałej warstwy pasywnej (tlenkowej) na powierzchni, gdy ma kontakt z tlenem. Ta niewidzialna warstwa działa jak naturalna bariera ochronna, zapobiegając dalszej korozji.
Czy stal nierdzewna jest całkowicie odporna na korozję? Niestety, nie ma materiałów absolutnie odpornych na wszystko. Stal nierdzewna wykazuje bardzo wysoką odporność w wielu środowiskach, ale w specyficznych warunkach, np. w obecności wysokich stężeń chlorków (woda morska, niektóre chemikalia) lub w bardzo kwaśnym środowisku, również może ulec korozji, np. w postaci wżerów. Mimo to, jest to jeden z najlepszych wyborów, gdy potrzebujemy materiału o wysokiej trwałości i odporności na niszczenie.
Inhibitory korozji: chemiczni "strażnicy" spowalniający proces niszczenia
Inhibitory korozji to substancje chemiczne, które dodawane do środowiska korozyjnego w niewielkich ilościach, potrafią spowolnić lub wręcz całkowicie zatrzymać proces niszczenia. Działają one na różne sposoby: mogą tworzyć ochronne warstwy na powierzchni metalu, zmieniać skład elektrolitu lub wpływać na reakcje anodowe i katodowe. Przykładem ich zastosowania są płyny chłodnicze w samochodach, które zawierają inhibitory chroniące elementy silnika przed korozją. Są również używane w przemyśle, np. w instalacjach wodnych czy gazowych, aby przedłużyć żywotność rurociągów.
Walka z korozją czy da się ją całkowicie zatrzymać?
Po poznaniu mechanizmów i metod ochrony, naturalnie nasuwa się pytanie: czy jesteśmy w stanie całkowicie wyeliminować korozję? Moje doświadczenie podpowiada, że to zadanie niezwykle trudne, a w wielu przypadkach wręcz niemożliwe. Korozja jest zjawiskiem naturalnym, dążeniem materiałów do powrotu do stanu równowagi termodynamicznej. Jednak to nie znaczy, że jesteśmy bezsilni.
Świadomość i prewencja jako klucz do długowieczności materiałów
Całkowite zatrzymanie korozji jest wyzwaniem, ale świadomość jej mechanizmów i konsekwencji, a także konsekwentne stosowanie metod prewencyjnych, są absolutnie kluczowe. Dzięki nim możemy znacząco wydłużyć żywotność materiałów i konstrukcji. Regularna konserwacja, odpowiedni dobór materiałów do środowiska, stosowanie powłok ochronnych czy systemów ochrony katodowej to inwestycje, które zwracają się wielokrotnie, zapobiegając kosztownym awariom i zapewniając bezpieczeństwo. To trochę jak dbanie o zdrowie nie wyeliminujemy wszystkich chorób, ale możemy znacznie zmniejszyć ryzyko, prowadząc zdrowy tryb życia i regularnie się badając.
Przeczytaj również: Jonizacja powietrza: Tajemnica świeżości? Wpływ na zdrowie i dom
Przyszłość walki z korozją: nowe materiały i technologie
Walka z korozją to obszar, który dynamicznie się rozwija. Naukowcy i inżynierowie nieustannie poszukują nowych, bardziej efektywnych rozwiązań. Obserwujemy badania nad nowymi, bardziej odpornymi materiałami, które z natury będą mniej podatne na niszczenie. Rozwijane są również inteligentne powłoki samonaprawiające się, które potrafią zasklepić drobne uszkodzenia, zanim korozja zdąży się rozwinąć. Coraz większe znaczenie mają także zaawansowane technologie monitorowania i zapobiegania korozji, wykorzystujące czujniki i sztuczną inteligencję do przewidywania i reagowania na zagrożenia. Wierzę, że te innowacje pozwolą nam w przyszłości jeszcze skuteczniej chronić nasze otoczenie przed niszczycielskim wpływem korozji.