Osmoza to jedno z najbardziej fundamentalnych zjawisk w biologii i chemii, które w dużej mierze kształtuje procesy życiowe na naszej planecie. Zrozumienie, czym jest i jak działa, pozwala nam dostrzec jego znaczenie w każdym zakątku natury od pojedynczej komórki, przez funkcjonowanie całych organizmów, aż po procesy technologiczne, które wykorzystujemy na co dzień. Jako Wiktor Cieślak, z przyjemnością oprowadzę Was po fascynującym świecie osmozy.
Osmoza to kluczowy proces życiowy zrozum, jak działa przepływ wody przez błony
- Osmoza to spontaniczny przepływ rozpuszczalnika (najczęściej wody) przez błonę półprzepuszczalną.
- Proces ten zachodzi od roztworu o niższym stężeniu substancji rozpuszczonej do roztworu o wyższym stężeniu, dążąc do wyrównania stężeń.
- Błona półprzepuszczalna przepuszcza wodę, ale zatrzymuje większe cząsteczki substancji rozpuszczonych.
- W zależności od stężenia roztworu, komórki mogą pęcznieć (roztwór hipotoniczny), kurczyć się (roztwór hipertoniczny) lub pozostawać bez zmian (roztwór izotoniczny).
- Osmoza jest fundamentalna dla życia roślin (pobieranie wody, turgor) i zwierząt (równowaga wodno-elektrolitowa).
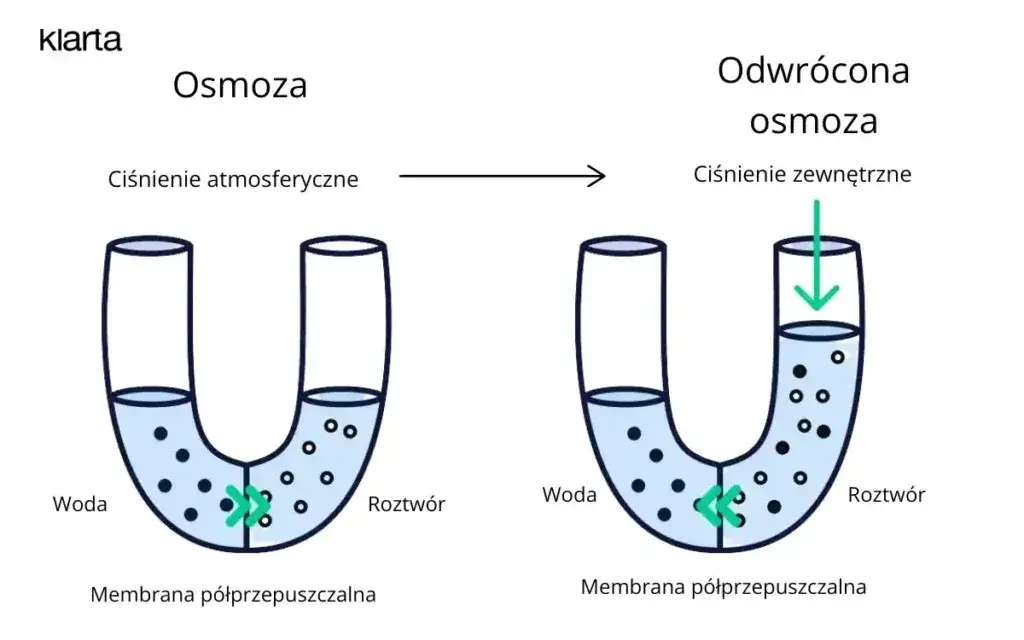
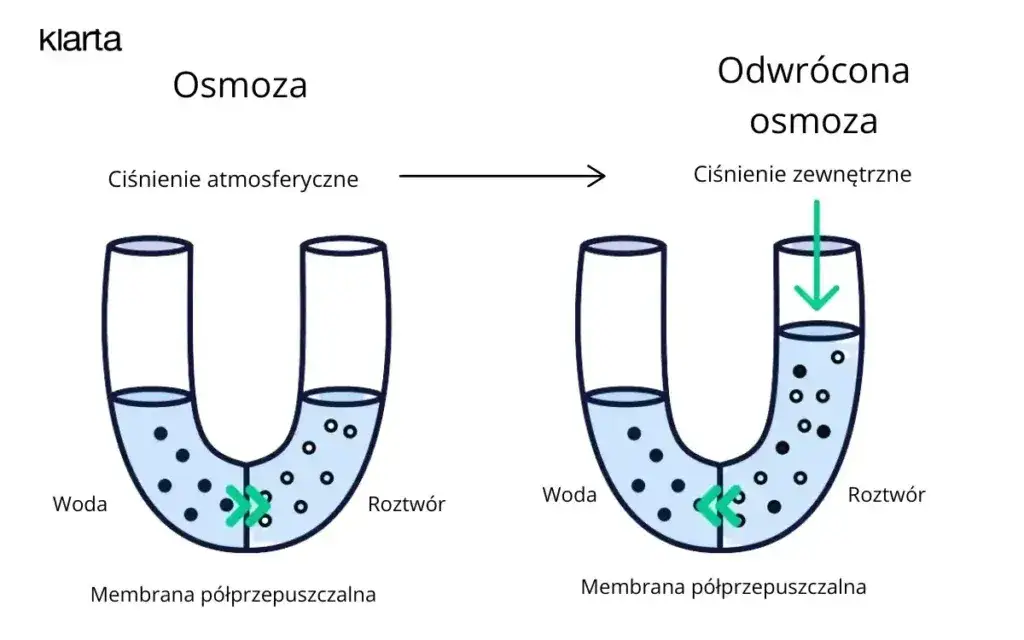
- Odwrócona osmoza to wymuszony proces wykorzystywany do odsalania wody czy filtracji.
Zrozumieć osmozę: Kluczowy proces w naturze
Osmoza to nic innego jak spontaniczny proces dyfuzji, czyli przepływu rozpuszczalnika w większości przypadków wody przez specjalną barierę, którą nazywamy błoną półprzepuszczalną. Ta błona rozdziela dwa roztwory o różnym stężeniu substancji rozpuszczonej. Kluczowe jest to, że woda zawsze dąży do wyrównania stężeń po obu stronach błony, przepływając od roztworu o niższym stężeniu substancji rozpuszczonej (czyli tam, gdzie jest więcej wolnej wody) do roztworu o wyższym stężeniu (gdzie cząsteczek wody jest proporcjonalnie mniej). To zjawisko jest absolutnie fundamentalne dla funkcjonowania każdej żywej komórki i ma ogromne znaczenie dla życia na Ziemi.
Trzy filary osmozy: Czego potrzebujesz, by zaszła?
Aby osmoza mogła zajść, potrzebujemy kilku kluczowych elementów, które działają ze sobą w harmonii. Bez nich ten niezwykle ważny proces byłby niemożliwy.
- Rozpuszczalnik (najczęściej woda): To on jest "bohaterem" osmozy, to jego cząsteczki przemieszczają się przez błonę. Woda jest uniwersalnym rozpuszczalnikiem w systemach biologicznych.
- Substancja rozpuszczona: Mogą to być sole mineralne, cukry czy białka. Jej obecność w rozpuszczalniku tworzy roztwór i generuje różnicę stężeń, która jest siłą napędową osmozy.
- Błona półprzepuszczalna: To selektywna bariera, która decyduje, co może przejść, a co musi zostać. Jest to serce mechanizmu osmotycznego.
- Różnica stężeń (gradient stężeń): To podstawowy warunek. Musi istnieć nierównowaga w stężeniu substancji rozpuszczonej po obu stronach błony, aby woda miała "motywację" do przemieszczania się i dążenia do równowagi.
Błona półprzepuszczalna: Strażnik komórkowego porządku
Błona półprzepuszczalna to prawdziwy strażnik, który decyduje o tym, co może wejść do komórki, a co musi pozostać na zewnątrz. Jest to membrana, która ma unikalną właściwość: przepuszcza cząsteczki rozpuszczalnika, takie jak woda, ale zatrzymuje większe cząsteczki substancji rozpuszczonych, na przykład cukrów czy soli. W organizmach żywych, taką rolę doskonale pełni błona komórkowa, która otacza każdą komórkę, chroniąc jej wnętrze i regulując wymianę substancji z otoczeniem.
Selektywna przepuszczalność, czyli kto może wejść, a kto musi zostać na zewnątrz
Koncepcja selektywnej przepuszczalności jest fascynująca. Błona komórkowa nie jest po prostu sitem. Jej zdolność do selektywnego przepuszczania cząsteczek wynika z jej złożonej budowy, głównie z podwójnej warstwy lipidowej i wbudowanych w nią białek. To właśnie rozmiar i właściwości chemiczne cząsteczek (np. ich ładunek elektryczny czy rozpuszczalność w tłuszczach) decydują o tym, czy mogą one swobodnie przejść przez błonę, czy też zostaną zablokowane. Woda, będąc małą i polarną cząsteczką, może stosunkowo łatwo przenikać przez błonę, natomiast większe cząsteczki, takie jak glukoza czy jony, potrzebują specjalnych kanałów lub transporterów, a w przypadku osmozy są zatrzymywane, co pozwala na powstanie gradientu stężeń.
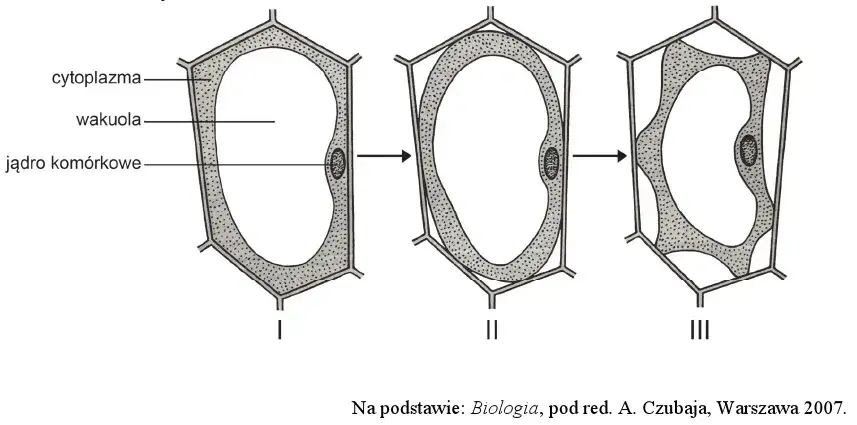
Wpływ roztworów na komórki: Co dzieje się w różnych środowiskach?
Kiedy komórka zostaje umieszczona w roztworze, jej los zależy od stężenia tego roztworu w porównaniu do stężenia wnętrza komórki. To właśnie ta różnica decyduje o kierunku przepływu wody i ostatecznie o kształcie, a nawet przetrwaniu komórki. Zrozumienie tych zależności jest kluczowe dla biologii.
Roztwór izotoniczny: Stan idealnej równowagi
Roztwór izotoniczny to taki, który ma takie samo stężenie substancji rozpuszczonych jak wnętrze komórki. Kiedy komórka znajdzie się w takim środowisku, przepływ wody przez błonę jest zrównoważony tyle samo wody wpływa do komórki, co z niej wypływa. W rezultacie, komórka nie zmienia swojej objętości ani kształtu. Dla komórek zwierzęcych, takich jak nasze krwinki, jest to idealne środowisko, zapewniające ich prawidłowe funkcjonowanie.
Roztwór hipotoniczny: Dlaczego komórka pęcznieje jak balon?
Roztwór hipotoniczny to roztwór o niższym stężeniu substancji rozpuszczonych niż wewnątrz komórki. W takiej sytuacji, zgodnie z zasadami osmozy, woda zaczyna intensywnie napływać do komórki, aby wyrównać stężenia. Komórka zaczyna pęcznieć. W przypadku komórek zwierzęcych, które nie posiadają sztywnej ściany komórkowej, nadmierny napływ wody może doprowadzić do ich pęknięcia, czyli hemolizy. Komórki roślinne, dzięki swojej sztywnej ścianie komórkowej, są bardziej odporne pęcznieją, ale nie pękają, a jedynie zwiększają swoje ciśnienie turgorowe, co nadaje im jędrność.
Roztwór hipertoniczny: Skutki dramatycznej utraty wody
Z kolei roztwór hipertoniczny charakteryzuje się wyższym stężeniem substancji rozpuszczonych niż wewnątrz komórki. W tym scenariuszu woda, dążąc do wyrównania stężeń, zaczyna wypływać z komórki. Skutkiem tego jest kurczenie się komórki. W komórkach zwierzęcych prowadzi to do ich marszczenia się i utraty funkcji. W komórkach roślinnych zjawisko to nazywamy plazmolizą błona komórkowa odrywa się od ściany komórkowej, a komórka traci jędrność, co widać na przykładzie więdnących roślin. To pokazuje, jak delikatna jest równowaga wodna w żywych organizmach.
Osmoza w akcji: Przykłady z życia codziennego i natury
Osmoza nie jest tylko abstrakcyjnym pojęciem z podręczników biologii. To zjawisko jest wszechobecne i odgrywa kluczową rolę zarówno w skomplikowanych procesach biologicznych, jak i w prostych, codziennych sytuacjach, które często ignorujemy. Pozwólcie, że pokażę Wam kilka przykładów, które najlepiej ilustrują jej działanie.
Królestwo roślin: Jak korzenie "piją" wodę i dlaczego warzywa więdną?
Rośliny są mistrzami w wykorzystywaniu osmozy. To właśnie dzięki temu procesowi korzenie roślin pobierają wodę z gleby. Komórki korzeni mają wyższe stężenie substancji rozpuszczonych niż woda w glebie, co sprawia, że woda osmotycznie napływa do ich wnętrza. Osmoza jest również odpowiedzialna za utrzymanie turgoru, czyli jędrności i sztywności komórek roślinnych. Kiedy roślina ma wystarczająco dużo wody, jej komórki są napęczniałe, a roślina stoi prosto. Jeśli jednak brakuje wody, komórki tracą turgor, a roślina więdnie to klasyczny przykład działania osmozy.
Nasze ciało: Osmoza jako strażnik równowagi wewnętrznej
W naszych organizmach osmoza jest absolutnie kluczowa dla utrzymania homeostazy, czyli wewnętrznej równowagi. Odpowiada za regulację gospodarki wodno-elektrolitowej w komórkach i płynach ustrojowych. Na przykład, nasze erytrocyty (czerwone krwinki) są niezwykle wrażliwe na zmiany stężenia środowiska. W roztworze izotonicznym czują się najlepiej, natomiast w roztworze hipotonicznym pęcznieją i pękają (hemoliza), a w hipertonicznym kurczą się. To pokazuje, jak precyzyjnie musi być kontrolowane stężenie płynów w naszym ciele.
Kuchenne eksperymenty: Od napęczniałej fasoli po pomarszczone palce w wannie
- Solenie mięsa dla konserwacji: Kiedy solimy mięso, tworzymy wokół niego roztwór hipertoniczny. Woda jest "wyciągana" z komórek mięsa, a także z komórek bakterii, co skutecznie hamuje ich rozwój i konserwuje żywność.
- Pomarszczone palce w wannie: Długa kąpiel sprawia, że woda z wanny (roztwór hipotoniczny w stosunku do komórek naskórka) wnika do komórek zewnętrznej warstwy skóry. Powoduje to ich pęcznienie i charakterystyczne marszczenie się.
- Pęcznienie fasoli lub grochu: Namoczenie suchych nasion w wodzie to klasyczny przykład. Woda osmotycznie wnika do nasion, powodując ich pęcznienie i zmiękczenie, co ułatwia późniejsze gotowanie.
- Więdnięcie warzyw posypanych solą: Jeśli posypiemy świeże warzywa solą, woda zostanie z nich "wyciągnięta" na zasadzie osmozy, co spowoduje ich szybkie zwiędnięcie.
Ciśnienie osmotyczne: Niewidzialna siła w przyrodzie
Ciśnienie osmotyczne to niezwykle ważny parametr, który pozwala nam ilościowo opisać "siłę" osmozy. Definiuje się je jako minimalne ciśnienie, które należy wywrzeć na roztwór o wyższym stężeniu, aby zatrzymać przepływ rozpuszczalnika przez błonę półprzepuszczalną. Innymi słowy, jest to miara "siły ssącej" roztworu im wyższe stężenie substancji rozpuszczonej, tym większe ciśnienie osmotyczne i tym silniej roztwór "przyciąga" wodę. To ciśnienie jest kluczowe dla wielu procesów biologicznych.
Turgor w komórkach roślinnych sekret jędrności i wzrostu
Turgor to stan, w którym komórki roślinne są wypełnione wodą, a ich błona komórkowa napiera na ścianę komórkową. To właśnie ciśnienie osmotyczne jest główną siłą napędową turgoru. Woda napływająca do komórek roślinnych zwiększa ich wewnętrzne ciśnienie, co sprawia, że roślina staje się jędrna i sztywna. Turgor jest absolutnie niezbędny dla roślin pozwala im utrzymać pionową postawę, wspiera wzrost, a także jest kluczowy w procesach otwierania i zamykania aparatów szparkowych, regulując wymianę gazową.
Odwrócona osmoza: Jak działa i do czego służy?
Odwrócona osmoza to fascynujący przykład, jak możemy wykorzystać naturalne zjawiska do celów technologicznych. W przeciwieństwie do naturalnej osmozy, która jest procesem spontanicznym, odwrócona osmoza jest procesem wymuszonym. Polega ona na zastosowaniu zewnętrznego ciśnienia, które jest wyższe niż naturalne ciśnienie osmotyczne, na roztwór o wyższym stężeniu. W ten sposób odwracamy naturalny kierunek przepływu rozpuszczalnika woda jest "przepychana" z roztworu o wyższym stężeniu do roztworu o niższym stężeniu, pozostawiając zanieczyszczenia po drugiej stronie błony.
Przeczytaj również: Kto odkrył promieniotwórczość? Prawda o Becquerelu i Marii Curie
Od odsalania wody morskiej po krystalicznie czystą wodę w Twoim domu
Zastosowania odwróconej osmozy są niezwykle szerokie i mają ogromne znaczenie dla współczesnego świata:
- Filtry do wody pitnej: Systemy odwróconej osmozy są powszechnie stosowane w domowych filtrach, aby usunąć z wody zanieczyszczenia, metale ciężkie, bakterie i wirusy, dostarczając krystalicznie czystą wodę.
- Odsalanie wody morskiej: To jedno z najważniejszych zastosowań. Odwrócona osmoza pozwala na przekształcenie słonej wody morskiej w wodę pitną, co jest kluczowe dla regionów cierpiących na niedobór wody.
- Demineralizacja wody: W przemyśle, laboratoriach czy medycynie potrzebna jest woda całkowicie pozbawiona minerałów. Odwrócona osmoza jest efektywną metodą uzyskiwania wody demineralizowanej.
- Przemysł spożywczy: Wykorzystuje się ją do koncentracji soków, mleka czy syropów, a także do oczyszczania ścieków.